《湖北省药品经营活动非现场检查指南》解读
一、起草必要性
一是贯彻落实国务院、省委和省政府一系列“放管服”改革工作举措的需要。非现场检查有利于降低书面资料审核风险,减少现场检查频次,从而减轻被检查企业检查负担,节约药品监管部门的经费。
二是创新药品监管方式和检查方法的需要。药品经营活动非现场检查相对于现场检查而言,可结合许可准入实行承诺告知制度,并根据首次许可、变更许可、延续许可风险大小发启,有利于提高监督检查的灵活性。
三是助力抗疫,为新冠疫情期间提供新的检查工具需要。对于因健康风险等危机因素不能实施现场检查的,确保药品监管工作不松、不断、不乱。
四是全面贯彻实施新修订《药品管理法》《药品检查管理办法》的需要。药品经营活动非现场检查指南是我省在全国药品监管系统首次出台的规范性文件,有利于推进药品智慧监管,是《湖北省药品经营活动检查指南》有益补充。
二、起草依据
(一)《药品管理法》《疫苗管理法》
(二)《药品检查管理办法(试行)》
(三)即将出台的《药品经营和使用监督管理办法》和《疫苗生产流通管理规定》等。
三、起草过程
本指南在起草过程中除依据上述法律、法规和规范性文件外,总结、吸收了国家药品监督管理局境外药品非现场检查经验,调研对全球药品监管机构采用非现场检查(远程检查、视频检查)的情况、程序与方法。特别是EMA药品GMP和GDP远程检查指南、英国在早些年就已经实施的GDP非现场检查监管经验。在我省已经发布《药品经营活动场地主文件编制指导原则》并建立完善了药品经营活动检查体系的前提下,充分研究了实施开展药品经营活动非现场检查的可行性。
起草指南草稿后,先后通过视频会议组织部分药品经营企业、省局分局、市州药品监管部门、省局相关处室进行集中讨论,2021年6月在省局官网公开征求意见。一经公开受到业内关注并给积极评价,目前国家局药品审核查验中心已将此种检查方式列为2021年创新药品检查方法。
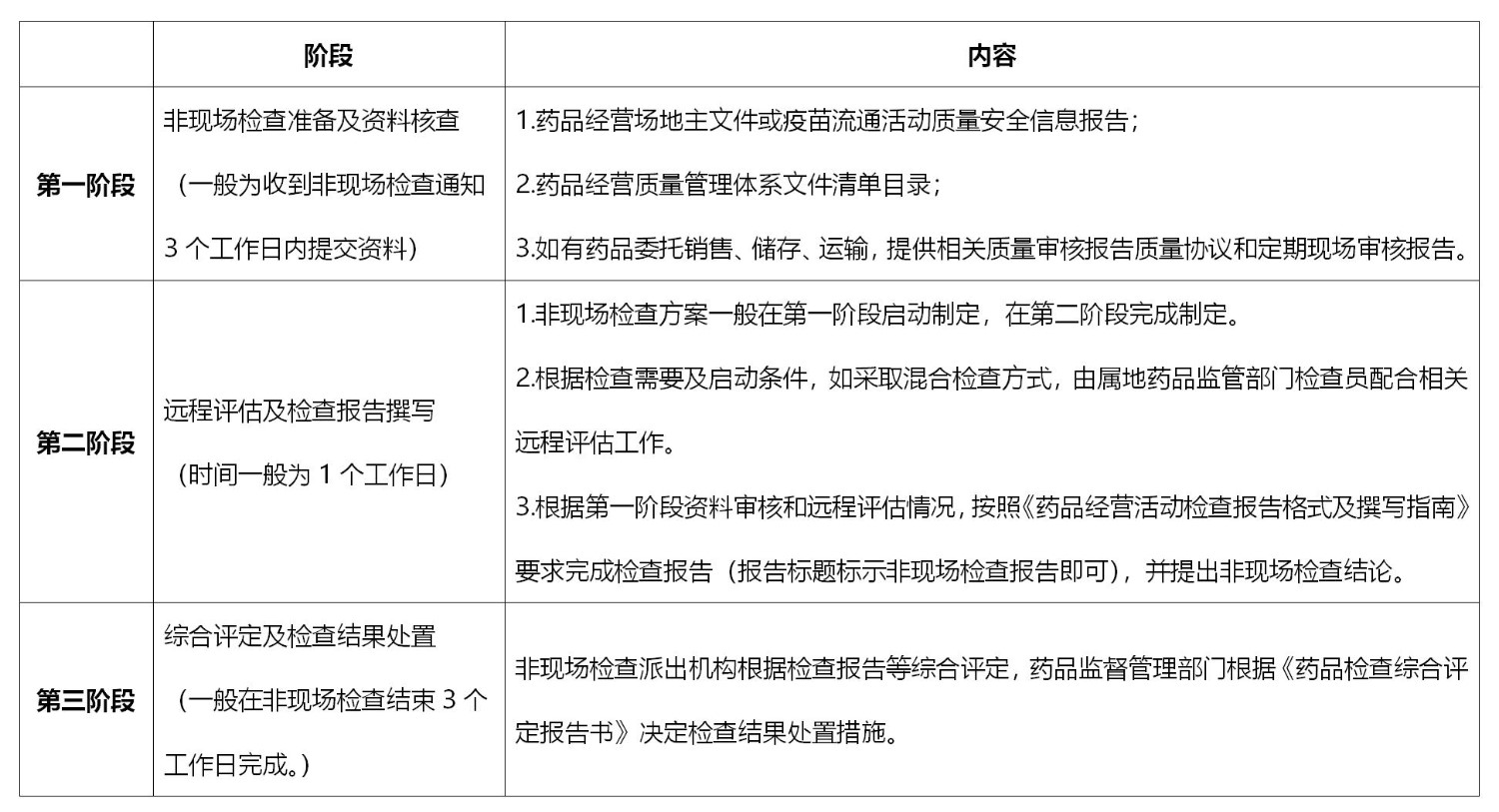
本指南在征求意见过程中未收到修改意见和建议。非现场检查实施流程如下:
相关附件:

 鄂公网安备42010602003442
鄂公网安备42010602003442 网站地图
网站地图