湖北省药品不良反应/事件监测年度报告(2023年)
| 索 引 号 | MB1529176/2024-17838 | 发文日期 | 2024-04-15 |
|---|---|---|---|
| 发布机构 | 湖北省药品监督管理局 | 文 号 | 无 |
| 分 类 | 食品药品监管 | 效力状态 | 有效 |
为全面反映2023年湖北省药品不良反应报告和监测情况,提高安全用药水平,促进临床合理用药,保障公众用药安全,湖北省药品监督管理局组织湖北省药品(医疗器械)不良反应监测中心(以下简称:省中心)编撰了《湖北省药品不良反应/事件监测年度报告(2023年)》。
第一章 总论分析
一、药品不良反应/事件报告总体情况
2023年,国家药品不良反应监测系统收到湖北省药品不良反应/事件报告97081份,较2022年增长19.65%。
(一)年度分布
2007-2023年,国家药品不良反应监测系统湖北省报告数稳步增长,目前累积数据已突破80万份,详见图1。
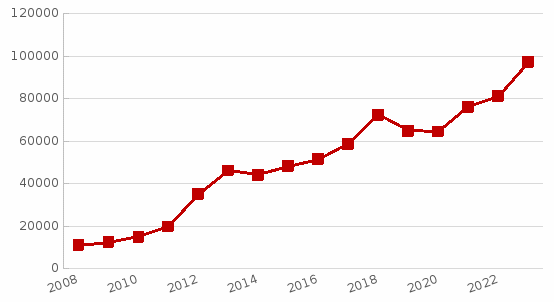
图1 2007-2023年湖北省药品不良反应/事件报告情况
(二)新的和严重的不良反应/事件报告
2023年,我省收到新的和严重的药品不良反应/事件报告37571份,占同期报告总数的38.70%,较2022年增长22.40%。其中,新的报告数为20195份,占同期报告总数的20.80%,较2022年增长15.59%;严重报告数为20100份,占同期报告总数的20.70%,较2022年增长28.35%。
(三)每百万人口平均报告数
每百万人口平均报告数是衡量各地区药品不良反应监测工作水平的指标之一。2023年,我省每百万人口平均报告数为1665.20份,与2022年相比上升18.53%。
(四)县(区)级报告比例
县(区)级药品不良反应/事件报告比例体现地区间药品不良反应监测工作发展均衡性及覆盖程度。2023年,我省县(区)级报告比例达100%。
(五)报告来源
2023年,我省药品不良反应/事件报告主要来源仍然是医疗机构,医疗机构报告主渠道地位持续上升,占比97.46%;药品经营企业占比2.49%;其他途径(计生机构、监测机构)也有少量报告。详见图2。
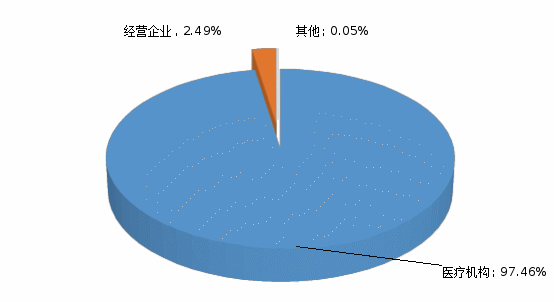
图2 药品不良反应/事件报告来源
(六)报告人职业
2023年,我省药品不良反应/事件报告上报人职业主要为医生,占比59.37%;其次为药师和护士,分别占比22.55%和15.07%。详见图3。
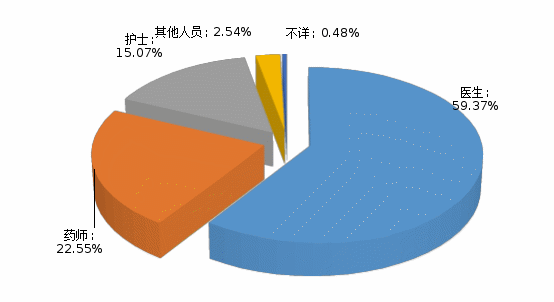
图3 药品不良反应/事件报告人职业构成
(七)药品不良反应/事件涉及患者情况
2023年药品不良反应/事件报告中,男女比例为0.79:1,女性多于男性。年龄分布从高到低依次是中年期、老年期、青壮年期和14岁以下儿童期。详见图4。
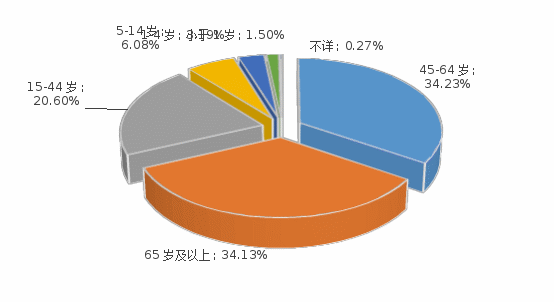
图4 药品不良反应/事件报告年龄分布
(八)涉及药品情况
按怀疑药品类别统计,化学药品占比88.87%,中药占比8.50%,生物制品占比2.63%。详见图5。
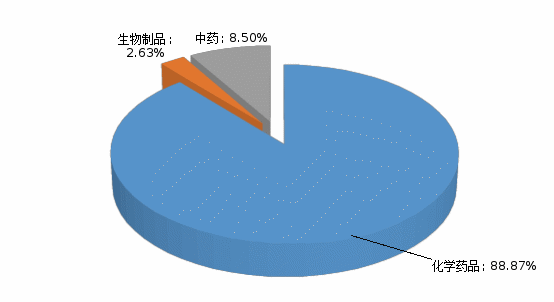
图5药品不良反应/事件报告涉及药品分类
按给药途径统计,静脉滴注依然是药品不良反应/事件报告的主要给药途径,占比64.54%,口服给药占比23.72%,其他注射给药途径(包括静脉注射、皮下注射、肌内注射、泵内注射等)占比6.76%,其他给药途径占比4.98%。详见图6。
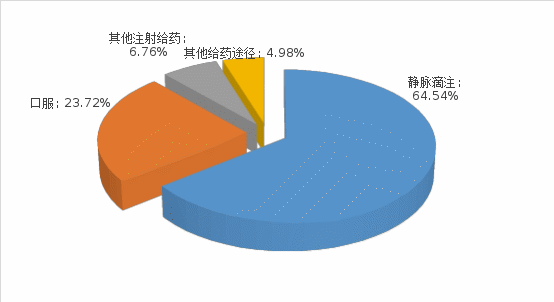
图6 药品不良反应/事件报告涉及给药途径分布
(九)药品不良反应/事件报告累及器官—系统情况
将药品不良反应名称按累及器官—系统分类,前5位的依次是皮肤及皮下组织类疾病、胃肠系统疾病、全身性疾病及给药部位各种反应、各类神经系统疾病和免疫系统疾病。详见图7。
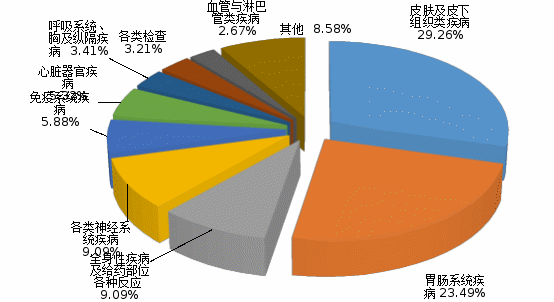
图7 药品不良反应/事件报告累及器官—系统
(十)药品不良反应/事件报告总体分析
2023年,全省药品不良反应/事件报告数量平稳增长,较上年同期增长19.65%,每百万人口平均报告数增长18.53%,严重报告增长28.35%。全省药品不良反应监测网络基层机构用户数量持续增加,县(区)级区域报告达到全覆盖;报告来源方面,医疗机构仍然是报告主体;给药途径主要是静脉滴注,其次为口服给药,两者共占比88.26%;年龄分布分析,以中年患者和老年患者为主,老年患者报告数呈持续走高态势,提示临床应持续加强对老年人群用药监测。
小贴士:什么是严重药品不良反应?
答:根据《药品不良反应报告和监测管理办法》(卫生部令第81号),严重药品不良反应是指因使用药品引起以下损害情形之一的反应:1)导致死亡;2)危及生命;3)致癌、致畸、致出生缺陷;4)导致显著的或者永久的人体伤残或者器官功能的损伤;5)导致住院或者住院时间延长;6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
二、化学药品、生物制品监测情况
(一)总体情况
2023年药品不良反应/事件涉及怀疑药品101623例次(怀疑药品为多个药品的,按多例报告统计)。其中,化学药品90315例次,占比88.87%;生物制品2675例次,占比2.63%;中药8633例次,占比8.50%。相比于2022年,化学药品上升20.57%,生物制品上升41.385%。
(二)药品情况
化学药品分类前5位分别是抗感染药(占比45.82%),肿瘤用药(占比9.90%),心血管系统用药(占比7.55%),神经系统用药(占比5.28%),电解质、酸碱平衡及营养药(占比4.43%),占总报告数的72.98%。严重报告中,抗感染药(占比40.51%)居首位,其次是肿瘤用药(占比21.39%)、心血管系统用药(占比4.81%)、神经系统用药与消化系统用药(占比3.79%),前5位类别共占比74.06%。
生物制品中,细胞因子占47.48%,抗毒素及免疫血清占13.01%,血液制品占5.05%,疫苗(含类毒素)占1.23%,其他生物制品占33.05%。
按给药途径统计,化学药品静脉给药、口服给药途径占比分别为71.13%和21.73%,其他给药途径占比7.14%;生物制品静脉给药、口服给药途径占比分别为58.80%和1.79%,其他给药途径(肌肉注射、皮下注射、泵内注射、皮内注射等)占比39.40%。
(三)总体情况分析
化学药品不良反应/事件报告主要为抗感染用药、肿瘤用药和心血管用药,与我国疾病谱的变化基本一致。化学药品品种分析发现,口服制剂中主要为心血管系统用药、精神障碍用药和抗感染用药;注射制剂中主要为抗感染用药和肿瘤用药,提示除关注感染性疾病、肿瘤外,还应关注心脑血管疾病及精神类等慢性疾病的用药安全。
小贴士:什么是药物过敏反应?
答:药物过敏反应又称之为变态反应,是致敏病人对某种药物的特殊反应。药物或药物在体内的代谢产物作为抗原与机体特异抗体反应或激发致敏淋巴细胞而造成组织损伤或生理功能紊乱。该反应仅发生于少数病人身上,和药物已知作用的性质无关,和剂量无线性关系,反应性质各不相同,不易预知,一般不发生于首次用药。初次接触时需要诱导期,停止给药反应消失,化学结构相似的药物易发生交叉或不完全交叉的过敏反应,某些疾病可使药物对机体的致敏性增加。药物引起的变态反应包括速发、迟发等4种类型,临床主要表现为皮疹、血管神经性水肿、过敏性休克、血清病综合征、哮喘等。对易致过敏的药物或过敏体质者,用药前应作过敏试验。
为了预防过敏反应,有关部门规定,有些药物如青霉素等应用前必须做皮试。但是有少数人皮试时就会发生过敏反应;有时皮试可能出现假阴性,极少数皮试阴性的病人也能发生过敏性休克;个别敏感患者甚至在别人注射青霉素时闻了一点气味,就发生了休克。特别要注意的是,许多没有规定作皮试的药物也可能引起过敏反应。对其它物质有过敏史的人,使用任何药品时都要非常谨慎。有药物过敏史的患者,在就医时,一定要把情况告诉医生,避免再服用同样或类似的药品。
三、中药监测情况
(一)总体情况
2023年,药品不良反应/事件报告涉及中药8633例次,总计909个品种。其中,严重报告1185例次,占严重报告总例次数的5.33%。
(二)药品情况
根据中药功能分类,不良反应/事件报告药品分类排名前5位的依次为理血剂(33.75%)、补益剂(13.46%)、清热剂(12.79%)、祛湿剂(12.35%)与开窍剂(3.98%),共占中药总例次数的76.33%。
中药严重药品不良反应/事件报告药品分类排名前5位依次是理血剂(占比46.06%)、补益剂(占比16.36%)、清热剂(占比11.33%)、祛湿剂(占比5.87%)与开窍剂(占比4.45%),共占比84.06%。
按给药途径统计,静脉给药占比37.28%,口服给药占比47.31%,其他给药途径占比15.42%。严重报告中,静脉给药占比66.41%,口服给药占比25.99%,其他给药途径占比7.6%。
(三)总体情况分析
2023年,中药药品不良反应/事件报告涉及药品主要为理血剂、补益剂、清热剂、祛湿剂。从给药途径分析,严重报告中静脉给药占比远高于中药总报告数占比,提示中药注射剂依旧为中药不良反应的主要风险点,应继续加大对中药注射剂的监测和管控。
小贴士:中药、西药一起吃,会不会增加不良反应?
答:中药、西药联用,有时能起到提高疗效、减少不良反应的目的,但是有时候合并用不一定能提高疗效,反而会增加不良反应,中西药联用的情况复杂,应充分听取医生的意见。
第二章 各论分析
一、国家基本药物监测情况分析
(一)总体情况
2023年,全省收到国家基本药物不良反应/事件报告47117份,占总报告数的48.53%,其中严重报告10287份,占国家基本药物报告数的21.83%。与2022年相比,国家基本药物不良反应/事件报告和严重报告数量分别上升19.29%和29.33%。
患者男女比例为0.78:1,与总体报告基本持平。年龄分布构成比从高到低依次为中年期患者(占比33.60%)、老年期患者(占比33.17%)、青壮年期患者(占比21.80%)及14岁以下儿童(占比11.43%)。
剂型分布中,注射制剂占比68.43%,口服制剂占比27.66%,其他制剂占比3.91%。
(二)化学药品和生物制品监测情况
《国家基本药物目录》(2018版)化学药品/生物制品部分25个类别,共417个(类)品种。2023年,我省收到国家基本药物化学药品/生物制品不良反应/事件报告40696份,占国家基本药物报告的86.37%,涉及43137例次(怀疑药品为多个药品的,按多例报告统计)、376个品种,其中严重报告9211份,涉及10259例次、296个品种。
按药品类别统计,报告数量排名前5位的依次是抗感染药(占比50.17%)、肿瘤用药(占比9.19%)、心血管系统用药(占比7.36%)、代谢及内分泌系统用药(占比4.94%)与消化系统用药(占比4.31%)。
不良反应累及器官—系统排名前5位的依次是皮肤及皮下组织类疾病(占比28.82%)、胃肠系统疾病(占比21.63%)、各类神经系统疾病(占比9.13%)、全身性疾病及给药部位各种反应(占比8.78%)、免疫系统疾病(占比7.03%)。
(三)中成药监测情况
《国家基本药物目录》(2018版)中成药部分7大类,共268个(类)品种。2023年,我省共收到国家基本药物中成药不良反应/事件报告3785份,占比8.03%,涉及3796例次、205个品种,其中严重报告528份,占国家基本药物严重报告数的5.13%,涉及528例次、92个品种。
2023年国家基本药物中成药中排名前五的类别为祛瘀剂(32.68%)、骨伤科用药(16.08%)、清热剂(12.87%)、扶正剂(7.45%)和温里剂(6.20%),多为内科用药。
不良反应累及器官—系统排名前5位的依次是胃肠系统疾病(35.22%)、皮肤及皮下组织类疾病(30.13%)、全身性疾病及给药部位各种反应(8.21%)、各类神经系统疾病(6.46%)、免疫系统疾病(5.43%)。
(四)安全性分析
2023年,我省国家基本药物监测情况平稳,化学药品/生物制品主要以抗感染药、肿瘤用药、心血管系统用药为主,其中抗感染药仍然居首位。中成药主要以内科用药、骨伤科用药和妇科用药为主。国家基本药物作为满足公众基本医疗需求的重要药品,需加强监测和管理。
小贴士:常用的抗感冒药有什么不良反应?
答:常用的抗感冒药多是由几种成分加在一起的复方药,其中经常含有扑热息痛、阿司匹林、双氯芬酸、布洛芬、扑尔敏、苯海拉明等,这些药物本身在不同程度上都能在一部分人身上引起不良反应,常见的不良反应有皮疹、嗜睡、消化道症状等;极少数患者使用还可能发生严重不良反应,如扑热息痛,曾有人报告发生了严重的肝脏损害、大疱性皮疹等,甚至有引起昏迷的;再如感冒通,少数人特别是儿童服用后出现血尿,应该引起重视。此外,抗感冒药多是复方制剂,使用时要避免含相同成分的不同药品联合使用,这种使用会加大抗感冒药的安全风险。
二、抗感染药物监测情况分析
(一)总体情况
2023年,全省收到抗感染药不良反应/事件报告37996份,占总报告数的39.13%。其中严重报告7957份,占抗感染药的20.94%,占严重报告总数的39.58%。与2022年相比,抗感染药不良反应/事件报告数量和严重报告数量分别上升27.98%和38.79%。
(二)患者情况
性别分布中,男女比例为0.79:1,与总体报告基本持平。年龄分布中,中年期患者占比居首位,其次为老年期、青壮年期和14岁以下儿童。
(三)药品情况
2023年抗感染药不良反应/事件报告涉及9大类别,抗生素居首位(占比61.65%),其次是合成抗菌药(占比29.51%)、抗病毒药(占比3.03%)、抗分枝杆菌药(占比2.48%)、天然来源抗感染药(占比1.72%)、抗真菌药(占比1.33%)、抗寄生虫药(占比0.12%)、其他抗感染药(占比0.09%)和消毒防腐药(占比0.07%)。抗生素分类中,排名前5名的药物类别依次是头孢菌素类、青霉素类、大环内酯类、林可霉素类和氨基糖苷类;合成抗菌药主要为喹诺酮类、硝基咪唑类。
剂型分布中,注射制剂占比88.32%,口服制剂占比8.71%,其他剂型占比2.97%。
(四)累及器官—系统情况
抗感染药不良反应/事件累及器官—系统损害排名前5位依次是皮肤及皮下组织类疾病(41.44%)、胃肠系统疾病(19.04%)、免疫系统疾病(9.27%)、全身性疾病及给药部位各种反应(7.82%)、各类神经系统疾病(6.09%)。
(五)安全性分析
抗感染药是指具有杀灭或抑制各种病原微生物作用的药品,是临床使用最为广泛的药品类别之一,其不良反应/事件报告数量一直居于首位,是药品不良反应监测工作关注的重点。2023年,抗感染药不良反应/事件报告数量和严重报告数量分别上升27.98%和38.79%,可能与2023年流感和支原体肺炎高发有关,排名前3位的依次是头孢菌素类、喹诺酮类和青霉素类,与临床用药较为广泛有关。剂型分布中,88%以上抗生素为注射剂,提示抗生素应用要选择合理的给药途径。
小贴士:为什么经过严格审批的药品,在正常用法用量情况下还会出现不良反应?
答:各国的新药审批主要依据动物实验和部分病人临床试验的结果。但是动物与人在生理、病理上有许多不同的地方;临床试验又存在观察时间短、参加人数少等局限性。许多发生率低、需要较长时间才能发现的不良反应,在审批时难以充分了解,所以许多经过严格审批的药品,在正常用法用量情况下还会引起不良反应,包括一些严重的不良反应。
三、肿瘤用药监测情况分析
(一)总体情况
2023年,全省收到肿瘤用药不良反应/事件报告共6426份,严重报告3194份。与2022年相比,不良反应/事件报告数量和严重报告数量分别上升14.85%,增长26.50%。
(二)患者情况
性别分布中,男女报告比例为0.82:1。年龄分布中,中年期占比50.89%,其次为老年期、青年期和儿童期。
(三)药品情况
2023年,肿瘤用药不良反应报告居前的品种依次为紫杉醇(14.08%)、奥沙利铂(9.40%)和顺铂(7.12%),可能与临床用药量大有关。肿瘤用药报告和严重报告中,以注射制剂为主。
(四)累及器官—系统情况
2023年肿瘤用药不良反应/事件累及器官—系统排名前5位的依次是胃肠系统疾病(25.96%)、血液及淋巴系统疾病(24.34%)、各类检查(18.19%)、全身性疾病及给药部位各种反应(7.85%)、皮肤及皮下组织类疾病(6.49%)。
(五)安全性分析
2023年,肿瘤用药较上年同期上升14.85%,低于总体报告增长水平,中年期患者占比居首位,多数肿瘤治疗药物治疗指数较窄,同时肿瘤患者的生理功能、药代动力学特征等易随着疾病的恶化而发生改变,所以抗肿瘤药物的ADR发生率高于其他药物,因此,应加强肿瘤患者用药后监测,了解肿瘤患者用药期间与药物相关的潜在危险,及时预防、发现和诊治抗肿瘤药引发的不良反应。
小贴士:哪些人易发生药品不良反应?
答:一般认为,老年人、妇女、儿童和有肝脏、肾脏、神经系统、心血管系统等方面疾病的人,容易发生药品不良反应。孕妇、哺乳期妇女服用某些药物还可能影响胎儿、乳儿的健康。
四、老年人用药监测情况分析
(一)总体情况
2023年,全省收到65岁以上老年人不良反应/事件报告33136份,占总报告数的34.13%。其中严重报告7173份,占老年人用药报告的21.65%,占严重报告总数的35.68%。与2022年相比,老年人用药报告数上升24.53%,严重报告数上升30.75%。
(二)患者情况
性别分布中,男女报告比例0.93:1,高于总体报告比例。年龄分布主要以65-74岁为主,占比60%以上,其次为75-79岁、80-84岁人群。
(三)药品情况
老年人用药中,化学药品/生物制品排名前5位的依次是抗感染药(占比38.20%),心血管系统用药(占比11.16%),肿瘤用药(占比9.41%),神经系统用药(占比6.71%),电解质、酸碱平衡及营养药(占比5.51%);中药排名前5位的依次是理血剂(占比50.13%)、补益剂(占比15.54%)、祛湿剂(占比8.50%)、清热剂(占比6.35%)和开窍剂(占比3.63%),与老年人的患病特征一致。
剂型分析中,注射制剂占比72.14%,口服占比23.67%,其他剂型占比4.19%。
(四)累及器官—系统情况
老年人用药中,化学药品/生物制品累及器官—系统排名前5位的是胃肠系统疾病(占比23.87%)、皮肤及皮下组织类疾病(占比22.66%)、全身性疾病及给药部位各种反应(占比10.59%)、各类神经系统疾病(占比10.10%)和心脏器官疾病(占比6.81%)。
(五)安全性分析
2023年监测数据显示,老年人用药报告数已连续3年呈增长趋势,以抗感染药、心血管系统用药、肿瘤用药最为常见。老年人群身体机能逐渐衰退,药物代谢速度降低,影响了老年患者用药。此外,老年人常患有多种慢性疾病,接受多种药物治疗的机会明显增加,多重用药、联合用药可明显增加因药物之间相互作用导致药品不良反应发生的风险。同时,老年患者药物不良反应存在不易识别和症状不典型的特点,难以与疾病进展相鉴别,因此老年患者需提高安全用药意识,减少药物错用、滥用、误用带来的危害,且重在用药过程的监测。
小贴士:特异质反应和哪些因素有关?
答:特异质反应又称特异性反应,是指个体对某些药物特有的异常敏感性。该反应可能和遗传有关,与药理作用无关,大多是由于机体缺乏某种酶,使药物在体内代谢受阻而致。如葡萄糖-6-磷酸脱氢酶(G-6-PD)缺乏者,服用伯氨喹、磺胺、呋喃妥因等药物可发生正铁血红蛋白血症,引起紫绀、溶血性贫血等。乙酰化酶缺乏者,服用异烟肼后易出现多发性神经炎,服用肼屈嗪后易出现全身性红斑狼疮样综合症。假胆碱脂酶缺乏者,使用琥珀酰胆碱后,由于延长了肌肉松弛作用而常出现呼吸暂停反应。
五、心血管系统用药监测情况分析
(一)总体情况
2023年,全省收到心血管系统用药不良反应/事件报告共6016份,严重报告908份。心血管系统用药报告占年报告数的6.20%,严重报告占心血管系统用药报告的15.09%,占严重报告总数的4.52%。与2022年相比,心血管系统用药报告数上升21.54%,严重报告上升40.99%。
(二)患者情况
性别分布中,男女报告比例0.87:1,高于总体报告比例。年龄分布中,老年期和中年期患者占比超过90%,是心血管用药的主要人群。
(三)药品情况
心血管系统用药严重报告累及器官—系统排名前5位的是各类神经系统疾病(21.70%)、胃肠系统疾病(20.39%)、皮肤及皮下组织类疾病(12.41%)、全身性疾病及给药部位各种反应(11.00%)和心脏器官疾病(9.66%)。
2023年心血管系统用药报告和严重报告中,注射制剂占比分别为39.42%和47.15%;口服制剂占比分别为59.70%和52.19%。
(四)累及器官—系统情况
心血管系统用药报告累及器官—系统排名前5位的是各类神经系统疾病(21.70%)、胃肠系统疾病(20.39%)、皮肤及皮下组织类疾病(12.41%)、全身性疾病及给药部位各种反应(11.00%)和心脏器官疾病(9.66%)。
(五)安全性分析
监测数据显示,45岁以上人群是心血管用药的主要人群,药品分类中,降脂药、降血压药不良反应报告最多,与用药人群基数较大有关;剂型分布中,口服制剂报告居多,提示应加强关注心血管系统口服制剂不良反应发生情况。
小贴士:什么是合理用药?
答:世界卫生组织1985年在内罗毕召开的合理用药专家会议上,把合理用药定义为:“合理用药要求患者接受的药物适合他们的临床需要、药物的剂量符合他们个体需要、疗程足够、药价对患者及其社区最为低廉。” WHO1987年提出合理用药的标准是:
(1)处方的药应为适宜的药物。
(2)在适宜的时间,以公众能支付的价格保证药物供应。
(3)正确地调剂处方。
(4)以准确的剂量,正确的用法和疗程服用药物。
(5)确保药物质量安全有效。
目前尚无一个公认明确的合理用药定义。绝对合理的用药也是难以达到的,一般所指的合理用药只是相对的,当今比较公认的合理用药是应包含安全、有效、经济与适当这4个基本要素。
有关说明
(一)本年度报告中的数据来源于国家药品不良反应监测数据库中2023年1月1日至2023年12月31日我省上报的数据。
(二)我国药品不良反应报告是通过自发报告系统收集并录入到数据库中的,也存在自发报告系统的的局限性,如漏报、填写不规范、信息不完善、无法计算不良反应发生率等。
(三)每种药品不良反应/事件报告的数量受到该药品的使用量和该药品不良反应发生率等诸多因素的影响,故药品不良反应/事件报告数量的多少不直接代表药品不良反应发生率的高低或者严重程度。
(四)本年度报告统计分析时采用的是监管活动医学词典(MedDRA)。MedDRA是在人用药品技术要求国际协调理事会(ICH)主持下编制的标准化国际医学术语集,用于与人用医疗产品相关的监管沟通和数据评估。各类检查是MedDRA中的一项系统器官分类,包括有限定词(例如:升高、降低、异常、正常)和没有限定词的检查名称。
(五)本年度报告完成时,其中一些严重报告等尚在调查和评价的过程中,所有统计结果均为数据收集情况的真实反映,有些问题并不代表最终的评价结果。
附件:

 鄂公网安备42010602003442
鄂公网安备42010602003442 网站地图
网站地图